Inloggen
Welkom op FTO
Log eenvoudig in met uw Medi-Access account
Nog geen account? Nu aanmelden
Wachtwoord vergeten?Maar liefst 500 personen per jaar sterven in Nederland aan de gevolgen van een chronische hepatitis B of C. Dit aantal is al jaren stabiel; het daalt niet ondanks de beschikbaarheid van praktisch perfecte therapie voor chronische hepatitis B (vanaf 2007) en chronische hepatitis C (vanaf 2014).
Is het mogelijk om Nederland vrij van hepatitissterfte te krijgen? Wellicht wel, via een actieve diagnose- en behandelstrategie.
De uitdaging voor de eerste lijn bestaat uit het (her)opsporen van patiënten met chronische hepatitis B of C, die in aanmerking komen voor behandeling. Want juist bij de behandeling van chronische virale hepatitis is grote gezondheidswinst te behalen. De uitdaging voor de tweede lijn bestaat uit het inzetten van de juiste behandeling en het identificeren van patiënten met een verhoogd risico op hepatocellulair carcinoom (leverkanker, HCC).
Deze publicatie gaat niet alleen in op bewustwording rondom chronische virale hepatitis. De auteurs besteden ook aandacht aan de diverse andere mogelijke oorzaken van hepatitis en de epidemiologie, de diagnostiek, de risicofactoren en de behandeling van virale hepatitis.
Hepatitis kan het gevolg zijn van diverse oorzaken, zowel viraal als niet-viraal. Bacteriën zijn zelden de oorzaak van hepatitis. Tabel 1 toont de belangrijkste oorzaken van hepatitis in Nederland.1
Tabel 1 Belangrijkste oorzaken van hepatitis in Nederland.
| Oorzaken van hepatitis | |
| Viraal | Niet-viraal |
| Hepatitis A-virus | Steatotische leverziekte (SLD) |
| Hepatitis B-virus | Alcohol-geassocieerde SLD (mannen >14 eenheden per week, vrouwen >10 eenheden per week) |
| Hepatitis C-virus | Metabool-geassocieerde SLD (MASLD) |
| Hepatitis E-virus | Geneesmiddelentoxiciteit |
| Auto-immuun |
Hepatitis kan ook veroorzaakt worden door de volgende, in Nederland veel minder vaak voorkomende, virussen:1
Tabel 2 Weinig voorkomende oorzaken van virale hepatitis in Nederland.
| Virus | Omschrijving |
| Hepatitis D-virus co-infectie | Dit virus is voor zijn vermenigvuldiging afhankelijk van het hepatitis B-virus. Zonder het hepatitis B-virus kan een hepatitis D-infectie niet bestaan. Zowel een co-infectie (een gelijktijdige besmetting met beide virussen) als een superinfectie (besmetting met het hepatitis D-virus bij een hepatitis B-drager) kan leiden tot een ernstige leverziekte. |
| Gele koorts virus | Deze komt alleen in de sub-Sahara-regio en in Zuid-Amerika voor; verspreiding vindt plaats via steekmuggen. Vaccinatie is de belangrijkste preventieve maatregel om de ziekte te bestrijden. |
| Epstein-Barr virus | Dit virus veroorzaakt vaak gestoorde levertesten, maar zelden icterus (gele verkleuring van de weefsels). |
| Humaan herpesvirus type 6 (HHV-6) | Dit virus komt vaak voor in de leeftijd van 6 tot 18 maanden, maar veroorzaakt zelden een acute icterische hepatitis. |
| Cytomegalovirus | Deze veroorzaakt vaak gestoorde levertesten, maar bij immuuncompetente personen geen icterus. |
Het is belangrijk om onderscheid te maken tussen acute en chronische virale hepatitis. Bij acute hepatitis ontwikkelt een van tevoren ‘lever-gezonde’ persoon één tot zes maanden na besmetting met een hepatitisvirus tekenen van leverontsteking. Ook kan acute hepatitis ontstaan ‘bovenop’ een chronische leverziekte door bijvoorbeeld MASLD.
Er is sprake van een chronische hepatitis als er langer dan zes maanden tekenen van leverontsteking zijn. Chronische hepatitis komt vrijwel alleen voor bij hepatitis B en C virusinfecties. Acute hepatitis A of E geneest vaak binnen enkele maanden, maar in zeldzame gevallen kan er ook een chronische hepatitis E virus infectie bestaan bij mensen met een ernstig verzwakt immuunsysteem, zoals transplantatiepatiënten. Acute hepatitis B geneest bij 95% van de volwassenen en kinderen ouder dan vijf jaar binnen zes maanden. Echter, bij jonge kinderen en neonaten gaat een subklinische hepatitis B, waarbij dus geen sprake is van merkbare klinische verschijnselen, in 50% - 90% van de gevallen over in een chronische hepatitis.1
Acute hepatitis C geneest in ongeveer 20% van de gevallen en wordt chronisch bij ongeveer 80% van de patiënten. Dit is onafhankelijk van de leeftijd.1
Acute hepatitis van het type A, B en C is in Nederland ‘zeldzaam’ geworden. De preventie van transmissie van hepatitisvirussen is in Nederland uitstekend.
Tabel 3 toont de incidentie van virale hepatitis A, B en C op basis van meldingen volgens de Wet publieke gezondheid.2
Tabel 3 Incidentie van virale hepatitis A, B en C in Nederland.
| Acute hepatitis: incidentie | |||||||||
| 2022 | 2021 | 2020 | 2019 | 2018 | 2017 | 2016 | 2015 | 2014 | |
| Hepatitis A | 93 | 77 | 50 | 163 | 181 | 362 | 77 | 79 | 105 |
| Hepatitis B | 87 | 74 | 96 | 105 | 85 | 110 | 79 | 108 | 141 |
| Hepatitis C | 28 | 34 | 44 | 74 | 47 | 59 | 41 | 70 | 53 |
Bron: RIVM2
Bij elkaar opgeteld gaat het de laatste jaren meestal om minder dan 250 gevallen per jaar. Aannemend dat ongeveer 30% van de klinische gevallen wordt gemeld, is het aantal acute hepatitis A, B en C gevallen in Nederland ongeveer 800 per jaar. Er zijn in Nederland ongeveer 8.000 huisartsen; een Nederlandse huisarts ziet dus gemiddeld eenmaal in de tien jaar een patiënt met acute virale hepatitis.1,3
Chronische hepatitis B en C komen veel vaker voor dan acute hepatitis. Chronische hepatitis B en, sinds 2019, ook chronische hepatitis C zijn meldingsplichtig. Tabel 4 geeft een overzicht van de prevalentie.
Tabel 4 Prevalentie van chronische hepatitis B en C in Nederland op basis van populatieonderzoek.
| Chronische hepatitis: prevalentie | ||
| % volwassenen | Totaal | |
| Hepatitis B | 0,24% | 40.000 |
| Hepatitis C | 0,16% | 22.800 |
Bron: Koopsen, 20193, Vriend, 20124
De prevalentie van chronische hepatitis B en C samen is ongeveer 0,4%. In een gemiddelde Nederlandse praktijk van 2.100 patiënten zijn er acht chronische dragers van het hepatitis B- of C-virus.3,4
Een deel van de chronische hepatitis B-dragers zijn inactieve HBsAg-dragers; sommige chronische hepatitis C-dragers zijn behandeld en genezen. Naar schatting is dat de minderheid, en zijn er in een gemiddelde Nederlandse huisartsenpraktijk vier patiënten met een actieve chronische hepatitis B of C.
De sterfte ten gevolge van acute hepatitis in Nederland was in de jaren 2002-2012 ongeveer zes personen per jaar.5
De sterfte door chronische hepatitis B en C bedraagt ongeveer 500 personen per jaar, zie figuur 1.6

Figuur 1 Sterfte door hepatitis in Nederland.
HBV = hepatitis B-virus
HCV = hepatitis C-virus
HCC = hepatocellulair carcinoom
* Tot en met 2012 werden de data handmatig geclassificeerd; vanaf 2013 vindt automatische classificering plaats.
Bij een ernstige klinische hepatitis is de ALAT meer dan 10 keer verhoogd. Er kan dan ook geelzucht ontstaan, veroorzaakt door een verhoogd bilirubine. Er zijn nog andere leverenzymtesten beschikbaar, zoals de ASAT en de GGT, deze zijn niet in de NHG-Standaard opgenomen.Specifieke lever-gerelateerde ziekteverschijnselen, zoals geelzucht, ascites en andere uitingen van een gevorderde of gedecompenseerde levercirrose komen relatief weinig voor. Deze ziekteverschijnselen worden weergegeven in figuur 2.1,7

Figuur 2 Ziektekenmerken van chronische hepatitis B en C.
Het eindstadium gedecompenseerde cirrose leidt tot een hoge sterfte ten gevolge van complicaties van portale hypertensie en een hoog risico op hepatocellulair carcinoom. Antivirale therapie is in dit eindstadium nog steeds mogelijk, en bij een deel van de patiënten levert dit gezondheidswinst op. Maar idealiter wordt er in een eerder stadium behandeld, zodat het ontstaan van cirrose kan worden voorkomen. Als er bij een patiënt sprake is van cirrose, is er een jaar na behandeling vaak een belangrijke afname van het ontstaan van gedecompenseerde cirrose. Ook het risico op hepatocellulair carcinoom neemt na effectieve behandeling langzaam af.8,9
Opsporing van asymptomatische actieve chronische hepatitis B en C is naast adequate behandeling van patiënten met leverziekteprogressie de grootste uitdaging om deze strategie te doen slagen.
Omdat specifieke symptomen vaak afwezig zijn lijkt de sleutel tot tijdige opsporing te liggen in het herkennen en testen van risicogroepen. Maar welke personen hebben nu een verhoogd risico en verdienen speciale aandacht?
Traditioneel is het risico op virale hepatitis gekoppeld aan risicocontacten. Hepatitis B wordt overgedragen door seksueel contact of contact met besmet bloed. Hepatitis C wordt vrijwel alleen overgedragen door bloedcontact.
Onderstaand kader toont een overzicht van de voornaamste risicocontacten voor hepatitis B en C.1
* dit zijn alle landen behalve Noordwest-Europa, Noord-Amerika, Australië en Nieuw-Zeeland.
De methode voor herkenning van risicocontacten werkt goed voor acute hepatitis, maar minder goed voor chronische hepatitis B en C.
Voor chronische hepatitis zijn daarom risicogroepen gedefinieerd op basis van een sterk verhoogde prevalentie van chronische hepatitis B of C.10-13
Onderstaand kader toont een overzicht van de voornaamste risicogroepen voor chronische hepatitis B en C.1
90% van de personen met chronische hepatitis B of C komt uit de bovengenoemde risicogroepen.
De prevalentie van chronische hepatitis B is met name hoog (meer dan 10%) in vele landen van Afrika, Polynesië, Nieuw-Guinea, Vietnam, Kirgizië en Zuidoost-Azië.1
Chronische hepatitis C komt veel voor (meer dan 3%) bij inwoners van Noord-Afrika. Binnen Europa komen zowel hepatitis B als hepatitis C veel voor in de voormalige Oostbloklanden. Met name in Polen en Roemenië kan de prevalentie oplopen tot 5-7%. Hepatitis C komt daarnaast relatief veel voor in Italië (~5,9%) en Griekenland (~2,2%).14
Tot 1982 zijn in Egypte miljoenen patiënten behandeld voor bilharzia met een serie injecties met kaliumantimoontartraat. Bilharzia is een infectieziekte die wordt veroorzaakt door de parasiet Schistosoma mansoni. Tijdens grote campagnes werden onvolledig gesteriliseerde spuiten en naalden gebruikt. Dit is waarschijnlijk de basis van een enorme verspreiding van het hepatitis C-virus, waarbij injecties, bloedtransfusie en chirurgische ingrepen nog steeds aan bijdragen. Personen die afkomstig zijn uit Egypte, en geboren zijn voor 1980, zouden daarom laagdrempelig onderzocht moeten worden op hepatitis C. De afgelopen jaren is er in Egypte enorme aandacht geweest voor hepatitis en de gevolgen hiervan. De combinatie van voorlichting en nieuwe behandelingen heeft ervoor gezorgd dat de incidentie van hepatitis C onder jongeren inmiddels vergelijkbaar is met die van West-Europa. Als deze ontwikkeling doorzet, kan Egypte in de komende jaren één van de eerste landen wereldwijd worden waar nog nauwelijks hepatitis C voorkomt.15
Bij personen die een tatoeage of piercing in een Westers land hebben laten aanbrengen of die een prikaccident hebben opgelopen in een Westers land, wordt geen verhoogd risico voor chronische hepatitis B of C meer gevonden.16
In de huisartsenpraktijk is het aantal personen met een risicofactor voor chronische hepatitis B of C opmerkelijk groot.
Immigranten vormen nu in Nederland 7% (4 tot 13%) van de totale bevolking.
Een ALAT >1,5 x normaalwaarde komt naar schatting voor bij 4% van de huisartsgeneeskundige populatie. Personen met risicocontacten vormen 1% van de huisartsgeneeskundige populatie.1,10,17
Bij elkaar heeft ongeveer 12% (9 tot 18%) van de bevolking een risicofactor voor chronische hepatitis B of C. In een gemiddelde huisartsenpraktijk van 2100 personen zijn dat 250 mensen. In de grote steden van West-Nederland is dit aantal groter dan in Noord-, Oost-, of Zuid-Nederland. Toch is het aantal personen met chronische hepatitis B of C in elke praktijk in het noorden, oosten en zuiden van Nederland nog steeds substantieel.
Om vast te stellen of iemand een hepatitis B-infectie heeft is alleen de HBsAg-test nodig. Er zijn diverse andere testen beschikbaar die voor de diagnostiek met betrekking tot hepatitis B gebruikt kunnen worden. Tabel 5 geeft hiervan een overzicht. Figuur 3 toont een afbeelding van het hepatitis B-virus.1
Tabel 5 Bloedonderzoek bij hepatitis B.
| Test | Uitslag |
| HBsAg | Positief of negatief |
| HBeAg | Positief of negatief |
| Anti-HBc | Positief of negatief |
| IgM-anti-HBc | Positief of negatief |
| Anti-HBs | IU/L |
| HBV-DNA | IU/L |
| Genotype | A,B,C,D,E,F |

Figuur 3 Het hepatitis B-virus.
Bij een positieve HBsAg-test is er sprake van een hepatitis B-infectie. Aanvullend onderzoek moet onderscheid maken tussen een inactieve en een actieve chronische hepatitis B, tenzij de klinische informatie van de arts over een recent risicocontact in de richting van een acute hepatitis wijst. In figuur 4 is dit onderzoek weergegeven.1

Figuur 4 Aanvullend onderzoek bij een positieve HBsAg test.
Bron: NHG-standaard Virushepatitis en andere leveraandoeningen1
Bijna altijd betreft het een chronische hepatitis B-infectie, tenzij er minder dan zes maanden geleden een risicocontact is geweest. Veel laboratoria volgen een doortestbeleid en doen automatisch een HBeAg-test.
Indien de HBeAg-test negatief is, is een HBV-DNA-test aangewezen. Pas indien HBV-DNA <2000 IU/L is en de ALAT-waarde normaal is, kan de diagnose ‘inactieve HBsAg-drager’ worden gesteld. Dit vervolgonderzoek dient in de regel in de tweede lijn te worden verricht.
Hepatitis C kan worden vastgesteld met een anti-HCV-test.
Voor het screenen op een hepatitis C-infectie is deze test meestal de eerste keuze.
Er zijn echter twee uitzonderingen:
In deze bijzondere gevallen is de HCV-RNA-test de test van keuze.
In specifieke gevallen kunnen medisch microbiologen aanvullend een genotype 1,2,3,4,5 of 6 test of een anti-HCV-immunoblot-test doen.
Een overzicht van hepatitis C-testen wordt getoond in tabel 6. Figuur 5 toont een afbeelding van het hepatitis C-virus.1
Tabel 6 Hepatitis C-testen.
| Test | Uitslag |
| Anti-HCV | Positief of negatief |
| HCV-RNA | Positief of negatief |
| Genotype | 1,2,3,4,5,6 |
| Anti-HCV immunoblot | Positief of negatief |

Figuur 5 Het hepatitis C-virus.
Een positieve anti-HCV-test betekent dat de patiënt een hepatitis C-infectie heeft of heeft gehad. Aanvullend onderzoek moet onderscheid maken tussen een actieve chronische hepatitis C en een doorgemaakte hepatitis C-infectie, tenzij de klinische informatie van de arts over een recent risicocontact in de richting van een acute hepatitis C wijst.1
Figuur 6 toont het aanvullende onderzoek dat bij een positieve anti-HCV-test plaats moet vinden.
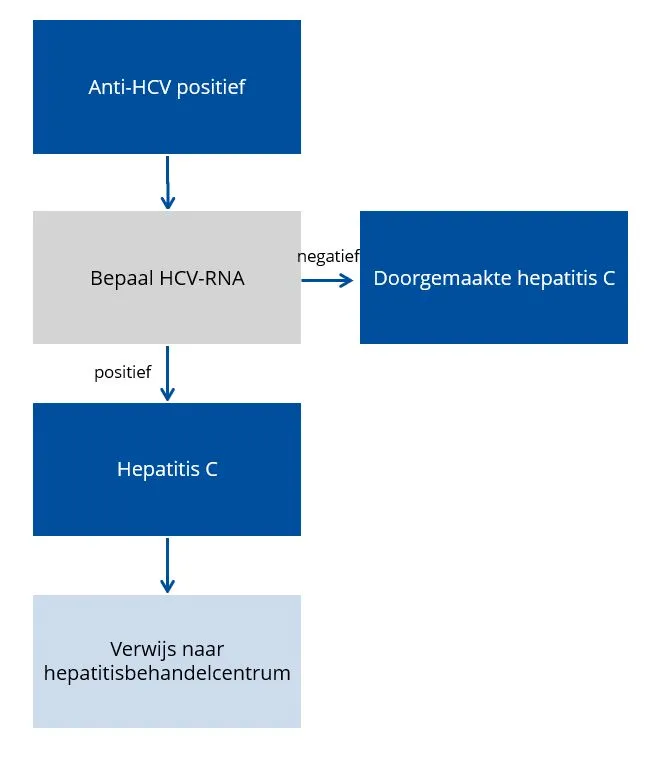
Figuur 6 Aanvullend onderzoek bij een positieve anti-HCV test.
Bron: NHG-standaard Virushepatitis en andere leveraandoeningen1
Bijna altijd betreft het een chronische hepatitis C-infectie, tenzij er minder dan zes maanden geleden een risicocontact is geweest.
Om te bevestigen dat een patiënt met een positieve anti-HCV-test een actieve hepatitis C-infectie heeft, moet de HCV-RNA-test positief zijn. De meeste laboratoria doen bij een positieve anti-HCV-test automatisch een HCV-RNA-test. Indien het HCV-RNA negatief is, heeft de patiënt het hepatitis C- virus geklaard.
Bij de beoordeling van een persoon met een positieve HBsAg- of anti-HCV-test, die de laatste zes maanden geen risicocontact heeft gehad, speelt de vraag of er bij deze patiënt sprake is van een potentiële indicatie voor antivirale therapie. Bij chronische hepatitis B is er sprake van een mogelijke indicatie voor antivirale therapie in het geval van een actieve chronische hepatitis B. Deze subgroep van actieve chronische hepatitis B-patiënten wordt gevormd op basis van twee additionele factoren:
Een schematisch overzicht wordt weergegeven in tabel 7.
Tabel 7 Subgroepen chronische hepatitis B: verantwoordelijke arts en acties.
| HBsAg | ALAT IU/L | HBV-DNA IU/L | Chronische HBV-categorie | % | Verantwoordelijke arts en actie |
| + | <66 | <2000 | Inactieve HBsAg-drager | 70 | Huisarts: halfjaarlijkse controle |
| + | >66 | >2000 | Chronische actieve HBV | 30 | Hepatitis-specialist: indicatie antivirale Rx, behandeling, controle |
Personen met een positieve HBeAg-test en/of HBV-DNA >2000 IU/ml hebben actieve virale replicatie en komen in aanmerking voor een beoordeling of antivirale therapie geïndiceerd is.
Personen met een normale ALAT waarde en HBV-DNA <2000 IU/ml zijn inactieve HBsAg-dragers, die nauwelijks een klinische ziekte hebben. Deze grote groep personen (50-70% van alle chronische HBsAg-positieven) kunnen, na beoordeling bij de hepatitis-specialist, bij de huisarts onder controle blijven. De NHG-Standaard stelt dat bij deze personen één tot tweemaal per jaar een ALAT en HBV-DNA dient te worden uitgevoerd en eenmaal per drie jaar een HBsAg-test.1
Per jaar wordt 1 tot 2% van de inactieve HBsAg-dragers actief; bij deze personen moet verwijzing naar een hepatitis-specialist (MDL-arts met speciale aandacht voor leverziekte of een internist met speciale aandacht voor infectieziekten) plaatsvinden. Deze specialist kan vervolgens beoordelen of voor deze patiënt antivirale therapie geïndiceerd is. Per jaar wordt ook 1 tot 2% van de inactieve HBsAg-dragers HBsAg-negatief; er is dan immuuncontrole over het hepatitis B-virus. De patiënt hoeft niet meer gecontroleerd te worden. Wel dient er rekening te worden gehouden met het risico van reactivatie, als behandeld wordt met immuunsuppresieve medicatie. In dergelijke gevallen dient altijd een hepatitis-specialist te worden geconsulteerd.
Bij patiënten met chronische hepatitis C is er een potentiële indicatie voor antivirale therapie als HCV-RNA aantoonbaar is. Een overzicht van de eventueel te nemen acties staat in tabel 8.
Tabel 8 Subgroepen chronische hepatitis C: verantwoordelijke arts en acties.
| Anti-HCV | HCV-RNA | Chronische HCV-categorie | % | Verantwoordelijke arts en actie |
| + | - | Doorgemaakte HCV | 30 | Huisarts: 1x bevestiging |
| + | + | Chronische HCV | 70 | Hepatitis-specialist: indicatie antivirale Rx, behandeling, controle |
Personen met een positieve anti-HCV-test maar een negatieve HCV-RNA-test hebben een HCV-infectie doorgemaakt en kunnen als genezen worden verklaard.
Alle personen met een positieve anti-HCV-test en een positieve HCV-RNA-test komen in aanmerking voor een beoordeling of antivirale therapie geïndiceerd is.
Antivirale therapie voor de behandeling van chronische hepatitis B bestaat in het algemeen uit:
Voor de behandeling van chronische hepatitis C worden direct antivirale middelen ingezet. Antivirale therapie voor de behandeling van chronische hepatitis C is in 2015-2016 veranderd van peginterferon-ribavirine naar ‘direct acting antivirals’ en bestaat meestal uit:
De meeste patiënten worden behandeld met één van deze combinatietherapieën. De kans op genezing is bijna 100%. Patiënten die falen op deze therapie kunnen veelal behandeld worden met de volgende combinatie van drie middelen:
De werkzaamheid van antivirale therapie voor chronische hepatitis B en chronische hepatitis C is zeer hoog (tabel 9).18,19 Werkzaamheid betekent remming van de virusreplicatie; HBV-DNA c.q. HCV-RNA zijn dan niet meer aantoonbaar en de leverontsteking verdwijnt.
Tabel 9 Werkzaamheid van hepatitis antivirale therapie tegen chronische hepatitis B en chronische hepatitis C.
| Kans | |
| Chronische hepatitis B | ≥95% volledige suppressie |
| Chronische hepatitis C | ≥95% genezing |
Deze medicamenteuze therapieën met zeer hoge werkzaamheid hebben doorgaans weinig bijwerkingen.
Bijwerkingen die klinisch relevant zijn door de ernst of door het vaker voorkomen in de therapiegroep dan in de placebocontrolegroep zijn de volgende:20
De therapie bij chronische hepatitis B is net als bij de behandeling van hiv, diabetes of hypertensie langdurig. Elk jaar kan maar 1 tot 2% van de chronische hepatitis-patiënten stoppen met de antivirale behandeling; dit zijn de patiënten die HBsAg-negatief zijn geworden. De jaarlijkse kosten van de behandeling van chronische hepatitis B zijn lager dan de kosten van antivirale therapie bij hiv-patiënten.
De duur van de therapie voor chronische hepatitis C is voor een groot deel van de patiënten 8-12 weken. Bij de juiste keuze van de combinatietherapie is na die tijd meer dan 95% van de patiënten genezen van de virusinfectie. De kosten van eenmalig 8-12 weken antivirale therapie voor hepatitis C zijn hoog, circa € 25.000 - 30.000. Toch is deze therapie zeer kosteneffectief gezien de grote gezondheidswinst, met name bij patiënten met cirrose.
Patiënten die zijn genezen van chronische hepatitis, maar die cirrose hebben, blijven een kleine kans houden op de ontwikkeling van een hepatocellulair carcinoom en moeten daarom onder halfjaarlijkse controle van een hepatitiscentrum blijven.
De uitdaging voor de eerste lijn betreft niet de behandeling zelf, maar veel meer de opsporing en heropsporing van de chronische hepatitispatiënten die in aanmerking komen voor behandeling. Dat is met een ziekte zonder duidelijke symptomen lastig.
De NHG-Standaard Virushepatitis en andere leveraandoeningen, herzien in februari 2023, vormt de basis voor het in figuur 7 getoonde stappenplan.1

Figuur 7 Stappenplan identificatie chronische hepatitis B of C in de huisartsenpraktijk.
Gerichte opsporing van chronische hepatitis B en C in de dagelijkse huisartspraktijk concentreert zich allereerst op spreekuurbezoekers afkomstig uit landen met een verhoogd risico, onafhankelijk van de klacht waarvoor zij komen. Het advies is om deze spreekuurbezoekers eenmalig te testen op chronische hepatitis B en C.
Daarnaast kan de huisarts, via het HIS of het huisartsenlaboratorium, patiënten identificeren met een verhoogde ALAT zonder duidelijke oorzaak en patiënten die ooit HBsAg of anti-HCV positief zijn geweest. Deze opsporing is praktisch lastig uitvoerbaar en kan onnodige onrust creëren bij patiënten en wordt daarom niet standaard aanbevolen in de richtlijn.
De rol van de huisarts bij opsporing is cruciaal. Eerder Nederlands onderzoek toonde aan dat een opsporingscampagne voor chronische hepatitis C effect heeft en kosteneffectief is als de huisarts hierbij wordt betrokken.21,22
Bij de opsporing van chronische hepatitis B of C bij drugsverslaafden en mannen die seks hebben met hiv-positieve mannen, spelen ook de GGD, verslavingszorg en het RIVM een belangrijke rol.
Om de huisarts te ondersteunen bij de opsporing van patiënten met chronische hepatitis B en C zijn er hulpmiddelen voor de praktijk ontwikkeld. In NHGDoc, een beslisondersteunend systeem dat operationeel is in het merendeel van de HIS-sen, is de module ‘Lever’ aangepast en krijgt de aangesloten huisarts een alert, bijvoorbeeld bij een positieve HBsAg of anti-HCV-test of bij een verhoogde ALAT, zonder verklarende ICPC-code.23
Via het HIS is het mogelijk een lijst te maken van patiënten met ICPC-codes 72.02-05; deze codes betreffen zowel acute als chronische hepatitis B en C. Daarnaast zijn er huisartsenlaboratoria, die een lijst van alle personen met een positieve HBsAg of anti-HCV-testen kunnen maken. Dit kan tot 10-15 jaar terug.
Zo kan ook een lijst van alle patiënten met een ALAT >1,5 x normaalwaarde zonder HBsAg en anti-HCV-uitslag gemaakt worden. Bij het huisartsenlaboratorium kan navraag worden gedaan naar deze mogelijkheden. Om deze ondersteuning overal operationeel te maken is overleg met huisartsenlaboratoria nodig.
Chronische hepatitis komt nog steeds relatief veel voor in Nederland. Een actieve diagnose- en behandelstrategie is noodzakelijk om hepatitissterfte terug te dringen. Zowel huisartsen als hepatitis-specialisten hebben hierin een belangrijke rol.
De uitdaging voor de eerste lijn betreft de opsporing en heropsporing van patiënten met chronische hepatitis B of C, die in aanmerking komen voor behandeling. Bewustwording van het bestaan van chronische hepatitis B en C in iedere huisartspraktijk, en van de mogelijkheid ziektelast en sterfte door cirrose te voorkomen, zijn daarbij belangrijke aandachtspunten voor de huisarts. Het herkennen van de specifieke risicogroepen is hierbij van wezenlijk belang.
De uitdaging voor de tweede lijn betreft de behandeling van chronische hepatitis. Er zijn verschillende goedgekeurde medicamenteuze behandelmogelijkheden. Het is soms lastig te bepalen welke therapie het meest geschikt is voor welke patiënt. De app TherapySelector en het HBV-richtsnoer kunnen helpen bij het maken van de juiste behandelkeuze.
Een 48-jarige, in Turkije geboren, vrouw, die sinds 1990 in Barendrecht woont en werkt, klaagt over een sinds lange tijd bestaande moeheid. Bij lichamelijk onderzoek vindt u een geringe, systolische souffle. Mevrouw heeft tevens enig overgewicht: haar BMI is 29. Oriënterend laboratoriumonderzoek laat geen afwijkingen zien. Mevrouw is in 2020, 2021 en 2022 opgenomen in het ziekenhuis op de afdeling cardiologie. Cardiologisch onderzoek toonde geen verklarende afwijkingen aan. Aanvullend laboratoriumonderzoek toont een ALAT-verhoging. De waarde is 121 IU/ml, terwijl deze normaal onder de 45 IU/ml moet zijn. De ALAT-verhoging was ook al in 2020, 2021 en 2022, tijdens de cardiologische opnames, vastgesteld.
Wat is uw beleid?
Bij personen die behoren tot een risicogroep voor chronische virale hepatitis en bij wie een herhaalde 1,5-10 maal verhoogde ALAT is geconstateerd is screening op chronische hepatitis B-C aangewezen. Bij deze mevrouw dient dan ook een HBsAg-test en een anti-HCV-test te worden uitgevoerd.
Een 19-jarige, in Nederland geboren, eerstejaarsstudente is in september met vakantie in Egypte geweest. Als zij terugkeert heeft zij een korte periode last van algehele malaise, weinig eetlust, gewrichtsklachten, zeer donkere urine en een lichte ontlasting. De menstruatie is normaal. Eind oktober maakt zij een afspraak met u, want ze voelt zich nog steeds niet goed. Bij lichamelijk onderzoek is er duidelijk sprake van een sclerale icterus. U vindt geen lever- of miltvergroting, wel bemerkt u een spider naevus op de schouder.
Wat is uw beleid?
U vraagt naar een risicocontact.
Risicocontacten voor hepatitis B en C zijn:
Bij een tevoren ‘lever-gezonde’ volwassene, die een land met een verhoogd hepatitisrisico bezoekt, en binnen 1-6 maanden tekenen van leverbeschadiging ontwikkelt, is screening op acute hepatitis aangewezen.
De volgende bepalingen dienen te worden gedaan:
Indien alle testen negatief zijn, doortesten met anti-EBVCA IgM, anti-CMV IgM, en anti-HEV IgM.
Bij een 52-jarige, in Suriname geboren man, die sinds 1982 in Nederland woont, is in de jaren ’90 van de vorige eeuw bij bloedtransfusiescreening vastgesteld dat hij HBsAg-positief is. Bij specialistisch onderzoek waren er geen tekenen van leverontsteking: de ALAT was <45 IU/L, de HBeAg-test was negatief en de HBV-DNA-waarde was <2000 IU/ml.
Patiënt was terugverwezen naar de huisarts en periodieke controles lieten tot nu toe een normale ALAT zien.
Situatie A.
Deze patiënt komt vanwege periodieke controle. Hij heeft niet gereisd en hij heeft geen overmatig alcohol, medicijnen of andere potentieel toxische middelen gebruikt. Bij lichamelijk onderzoek vindt u geen opvallende afwijkingen. Wel is zijn gewicht wat toegenomen, van 92 kg naar 98 kg. Laboratoriumonderzoek toont een ALAT van 121 IU/L.
Wat is uw beleid?
Volgens de tekst van de NHG-Standaard Virushepatitis en andere leveraandoeningen1 dient u te verwijzen naar een specialist leverziekten. Volgens de bedoeling van de NHG-standaard is een bij herhaling verhoogde ALAT of een door actieve HBV-replicatie veroorzaakte ALAT pas reden voor verwijzing. Bij deze patiënt herhaalt u de ALAT-test met het verzoek om bij herhaalde verhoging door te testen op HBV-DNA. U kunt ook de ALAT-test herhalen en bij een herhaalde verhoging doorverwijzen naar een specialist.
Situatie B.
De patiënt komt vanwege geelzucht. Hij heeft niet gereisd en hij heeft geen overmatig alcohol, medicijnen of andere potentieel toxische middelen gebruikt. Bij lichamelijk onderzoek vindt u geen opvallende afwijkingen. Wel is zijn gewicht wat toegenomen, van 92 kg naar 98 kg. Oriënterend laboratoriumonderzoek toont een bilirubinegehalte van 170 micromol/l, en een ALAT van 121 IU/L.
Wat is uw beleid?
Bij een ALAT-verhoging en een icterus dient u direct door te verwijzen naar een specialist leverziekten, want de ernstige klinische situatie van icterus wordt waarschijnlijk veroorzaakt door hepatitis B reactivatie.
Een 28-jarige, in Nederland geboren, ongetrouwde man die in dienst is van een slopersbedrijf en die bokst en in het weekend ‘stapt’, klaagt over een sinds lange tijd bestaande moeheid. Bij lichamelijk onderzoek ziet u een sterk gespierde man met tatoeages en enig overgewicht: een BMI van 26. Oriënterend laboratoriumonderzoek toont een geringe lymfocytose en een ALAT-verhoging: 78 IU/ml (de normaalwaarde is <45 IU/ml).
Wat is uw beleid?
Deze patiënt behoort tot een risicogroep chronische hepatitis B of C. Conform de geest van de NHG-Standaard is screening op chronische hepatitis B-C (dit betreft HBsAg en anti-HCV) aangewezen bij een 1,5-10 x verhoogde ALAT en bij het behoren tot een risicogroep chronische virale hepatitis.
Een 31-jarige in Mongolië geboren vrouw is revalidatiearts in een ziekenhuis. Wegens ziekte werkt zij al een paar maanden niet. Er is sprake van ascites en op de echo zijn tekenen van cirrose zichtbaar. Er wordt een behandeling met diuretica gestart, waarna de ascites afneemt.
Twee jaar later meldt patiënte zich opnieuw met klachten en blijkt er sprake te zijn van hepatocellulair carcinoom.
Wat valt u op als u deze geschiedenis leest?
Bij deze casus valt op dat bij deze patiënte in eerste instantie alleen symptomatische therapie is toegepast. Er is gekozen voor symptomatische behandeling van de acites, waarbij niet is gekeken naar de oorzaak van de cirrose. Een infectie met hepatitis B is hierdoor onbehandeld gebleven.
Bij de behandeling van cirrose is therapie die de oorzaak wegneemt vele malen effectiever dan symptomatische therapie. Bij een gedecompenseerde cirrose door een hepatitis B-infectie is antivirale therapie met tenofovir of entecavir, 1 tablet per dag, de basis. Zelfs bij gedecompenseerde cirrose verbeteren twee op de drie patiënten nadat de virusreplicatie onderdrukt is.
1. Auwerda J, Boelman L, Bouma M, et al. NHG-standaard Virushepatitis en andere leveraandoeningen. https://richtlijnen.nhg.org/standaarden/virushepatitis-en-andere-leveraandoeningen. Geraadpleegd: april 2024.
2. RIVM. Registratie infectieziekten. Meldingen wet publieke gezondheid. Opgevraagd: maart 2024.
3. Koopsen J, van Steenbergen JE, Richardus JH, et al. Chronic hepatitis B and C infections in the Netherlands: estimated prevalence in risk groups and the general population. Epidemiol Infect. 2019; 147:e147.
4. Vriend HJ, van de Laar TJ, Urbanus AT, et al. Hepatitis C virus seroprevalence in the Netherlands. Eur J Public Health. 2012;22:819-21.
5. Centraal Bureau Statistiek. http://statline.cbs.nl/statweb/. Geraadpleegd: juli 2019.
6. Hofman R, Nusselder WJ, Veldhuijzen IK, et al. Sterfte aan chronische hepatitis B en C virusinfectie in Nederland NTvG 2016;160:D511.
7. Hoofnagle JH. Hepatitis C: The Clinical Spectrum of Disease – Hepatology. 1997;26:Suppl.1,15S-20S.
8. Peng CY, Chien RN, Liaw YF, et al. Hepatitis B virus-related decompensated liver cirrhosis: benefits of antiviral therapy. J Hepatol. 2012; 57:442-50.
9. Curry MP, O’Leary JG, Bzowej N, et al. Sofosbuvir and velpatasvir for HCV in patients with decompensated cirrhosis. N Eng J Med 2015: 373:2618-28.
10. Marschall T, Kretzschmar M, Mangen MJ, et al. High impact of migration on the prevalence of chronic hepatitis B in the Netherlands. Eur J Gastroenterol Hepatol. 2008;20:1214-25.
11. Vriend HJ, van Veen MG, Prins M, et al. Hepatitis C virus prevalence in The Netherlands: migrants account for most infections. Epidemiol. Infect. 2013; 141:1310-17.
12. Arnold DT, Bentham LM, Jacob RP, et al. Should patients with abnormal liver function tests in primary care be tested for chronic viral hepatitis: cost minimisation analysis based on a comprehensively tested cohort. BMC Fam Pract. 2011;12:9.
13. Helsper C, van Essen G, Frijling BD, et al. Follow-up of mild alanine aminotransferase elevation identifies hidden hepatitis C in primary care. Br J Gen Pract. 2012;62:e212-6.
14. ECDC: Prevalentie hepatitis B en C. https://www.ecdc.europa.eu/sites/default/files/media/en/publications/Publications/systematic-review-hepatitis-B-C-prevalence.pdf. Geraadpleegd: maart 2024.
15. Hassanin A, Kamel S, Waked I, et al. Egypt's Ambitious Strategy to Eliminate Hepatitis C Virus: A Case Study. Glob Health Sci Pract. 2021;9(1):187-200.
16. Ditah I, Ditah F, Devaki P, et al. The changing epidemiology of Hepatitis C Virus infection in the United States: National Health and Nutrition Examination Survey 2001 through 2010. J Hepatol. 2013;60:691-698.
17. Wolffram I, Petroff D, Bätz O, et al. Prevalence of elevated ALT levels, HBsAg and anti-HCV in primary care setting. JHepato 2015:62:1256-64.
18. Tsai MC, Lee CM, Chiu KW, et al. A comparison of telbivudine and entecavir for chronic hepatitis B in real-world clinical practice. J Antimicrob Chemother. 2012;67:696-9.
19. Sulkowski MS, Gardiner DF, Rodriguez-Torres M, et al. Daclatasvir plus sofosbuvir for previously treated or untreated chronic HCV infection. N Eng J Med. 2014;370:211.
20. TherapySelector app. www.therapyselector.nl. Geraadpleegd: januari 2024.
21. Helsper CW, van Essen GA, Bonten MJ, et al. A support programme for primary care leads to substantial improvements in the effectiveness of a public hepatitis C campaign. Fam Pract. 2010; 27:328-32.
22. Helsper CW, Borkent-Raven BA, de Wit NJ, et al. Cost-effectiveness of targeted screening for hepatitis C in the Netherlands. Epidemiol Infect. 2012;140:58-69.
23. NHGdoc Hepatitis. https://www.nhgdoc.nl/over-nhgdoc/nhg-standaarden/hepatitis/. Geraadpleegd: maart 2024.